Descubriendo el funcionamiento del sistema de ósmosis

La ósmosis es un proceso fisicoquímico muy importante en la vida cotidiana. Tiene lugar cuando dos soluciones con diferentes concentraciones se separan por una membrana semipermeable. La solución con la mayor concentración se denomina solución hipotónica, mientras que la solución con la menor concentración se denomina solución hipertónica. Esta membrana permite que el agua pase a través de ella, pero no a la sal. Esto significa que el agua se mueve de la solución hipotónica a la solución hipertónica. Esto se denomina difusión osmótica.
Para entender mejor el proceso de ósmosis, vamos a considerar un ejemplo. Supongamos que tenemos dos recipientes con agua salada. El primer recipiente contiene una solución hipotónica con una concentración de sal relativamente baja. El segundo contiene una solución hipertónica con una concentración de sal relativamente alta. Si colocamos una membrana semipermeable entre los dos recipientes, el agua se moverá desde el primer recipiente hacia el segundo. Esto se debe a que el agua se moverá desde una solución hipotónica con una concentración más baja de sal hacia una solución hipertónica con una concentración más alta de sal.
El proceso de ósmosis se aplica a muchos aspectos de la vida cotidiana. Por ejemplo, se utiliza en la industria del agua para producir agua potable. El agua de mar, que es una solución hipertónica, se separa del agua dulce, que es una solución hipotónica, mediante una membrana semipermeable. El agua dulce se recoge en un lado de la membrana, mientras que el agua de mar se recoge en el otro lado. La ósmosis también se utiliza en la industria de los alimentos para separar los líquidos de los sólidos.
En conclusión, la ósmosis es un proceso fisicoquímico muy importante que se utiliza en muchos aspectos de la vida cotidiana. Está relacionado con el movimiento del agua a través de una membrana semipermeable desde una solución hipotónica (con una concentración de sal relativamente baja) hacia una solución hipertónica (con una concentración de sal relativamente alta).
Filtros de agua

BRITA Jarra con filtro de agua Marella blanca (2,4 l) incl. 3x cartuchos MAXTRA PRO All-in-1: jarra apta para frigorífico con memo digital y tapa abatible que reduce el cloro, la cal y las impurezas
- Reduce micro plásticos, cloro y metales pesados, agua filtrada de calidad, solución más sostenible
- Capacidad total 2,4 litros
- BRITA Memo digital mide el tiempo para recordar el cambio de filtro
- Fácil llenado con una sola mano con la tapa abatible
- 150 l de agua recién filtrada en 4 semanas con un solo cartucho


Philips Water Cartuchos de filtro de agua de repuesto, pack de 6 filtros, compatible con Brita, reduce los MICROPLÁSTICOS, el CLORO, la CAL, los METALES PESADOS
- Compatible con todas las jarras y dispensadores de agua Philips Water y todas las jarras Brita (Maxtra, Maxtra+, Perfectfit)
- Filtracion avanzada filtro Philips Micro X-Clean: reduce eficazmente las sustancias no deseadas tales como los microplásticos, el cloro, la cal, los metales pesados, los PFOA y otros contaminantes
- Filtración: tecnología de alto rendimiento que permite una filtración del agua rápida y reducción de la cal
- Prolonga la vida útil de los aparatos de cocina al evitar la acumulación de cal y mejora el sabor de sus bebidas y comidas favoritas
- Bueno para el medio ambiente: cada filtro dura 60 días y ahorra hasta 200 botellas de plástico (500ml)
- Hasta 6 meses de agua fresca: cada cartucho dura aproximadamente 1 mes o 100 l


BRITA ON TAP Pro V-MF Sistema de filtración de agua, incl. 1 cartucho filtrante (600L) - para agua 99,99% libre de bacterias y sostenible con una tecnologia de filtración para un excelente sabor
- Así de sencillo: ENROSCA en cualquier grifo, FILTRA y BEBE agua de buen sabor al instante. Se acabó cargar con botellas de agua.
- Más seguro: la filtración en 5 pasos detiene el 99,99% de las bacterias y reduce las micropartículas más finas, el cloro y otras sustancias que alteran el olor y el sabor, como el plomo y el cobre.
- Puedes elegir entre 3 cómodos modos para todo lo que necesites hacer en la cocina: agua filtrada (del tiempo) y agua sin filtrar (chorro normal y modo ducha)
- Inteligente: la pantalla LCD digital muestra la capacidad restante en tiempo real y indica cuándo tienes que cambiar el filtro - después de haber filtrado 600L de agua
- La sostenibilidad fácil: Di adiós a las botellas de plástico y disfruta de agua recién filtrada siempre disponible por sólo 4 céntimos el litro.
- Fácil instalación y cambio de filtro: compatible con la mayoría de grifos estándar (5 adaptadores incluidos) y puede montarse sin herramientas. Para cambiar el filtro, basta con desenroscar, extraer y sustituir el cartucho.
- "Mucho más que beber: gracias a la reducción de bacterias y a la mejora del sabor, el agua filtrada ON TAP también es óptima para cocinar. "
- Conserva valiosos minerales: no reduce la cal, pero conserva los minerales como el magnesio y el calcio
- Incluye: 1x sistema de filtración de agua del grifo BRITA ON TAP Pro V-MF, 1x cartucho filtrante ON TAP V-MF (600L), 5x adaptadores diferentes para la instalación
- Nota! 5 adaptadores de grifo: 2 x 22 mm, 1 x 23 mm, 1 x 24 mm, 1 x 15-25 mm.


Waterdrop 10UA Sistema de Filtro de Agua para Debajo del Fregadero, 30.000 Litros Sistema de Filtrado de Agua de Alta Capacidad, Certificado NSF/ANSI 42, Reduce el 99,99% de Plomo, Cloro, Mal Sabor
- 【Vida útil ultralarga】 Cuando se utiliza con agua municipal, cada filtro tiene una vida útil máxima de 12 meses o 30 000 litros. [1] 𝐍𝐨 𝐝𝐢𝐬𝐦𝐢𝐧𝐮𝐲𝐚 𝐞𝐥 𝐓𝐃𝐒. 𝐒𝐢 𝐝𝐞𝐬𝐞𝐚 𝐫𝐞𝐝𝐮𝐜𝐢𝐫 𝐥𝐚 𝐝𝐮𝐫𝐞𝐳𝐚 𝐝𝐞𝐥 𝐚𝐠𝐮𝐚 𝐨 𝐞𝐥 𝐓𝐃𝐒, ¡𝐞𝐥𝐢𝐣𝐚 𝐞𝐥 𝐬𝐢𝐬𝐭𝐞𝐦𝐚 𝐖𝐚𝐭𝐞𝐫𝐝𝐫𝐨𝐩 𝐑𝐎!
- 【Filtración multietapa innovadora】 El sistema de filtración de agua debajo del fregadero Waterdrop Direct Connect utiliza una filtración multietapa innovadora. Y puede reducir eficazmente el cloro, los metales pesados, las impurezas químicas, los sedimentos y otras partículas grandes.[2]
- 【Filtro certificado NSF】 Los materiales premium especialmente seleccionados no contienen plomo, lo que está totalmente certificado por WQA según el estándar NSF 372. mantiene el filtro higiénico de manera efectiva. Probado según los estándares NSF 42, reduce eficazmente el cloro, el sabor y el olor. El material sin BPA y sin plomo garantiza un uso más confiable de adentro hacia afuera.
- 【Instalación simple】 El sistema solo debe conectarse a una red de agua fría. Todo el proceso de instalación lleva menos de 3 minutos. El diseño de giro y bloqueo garantiza que el filtro se pueda cambiar en 3 segundos. El sistema incluye una manguera de 3/8". El accesorio convertidor de 3/8" – 1/2" permite conectar el sistema a líneas y grifos de agua fría de 1/2" y 3/8".
- 【Flujo rápido y usos múltiples】 El suministro de agua rápido y estable proporciona agua pura con sabor a agua de manantial. El caudal máximo probado es de 9,0 litros/minuto a 60 psi. Desarrollado para uso doméstico y comercial, el sistema de filtro de agua debajo del fregadero se puede instalar en la cocina, el baño, el vehículo recreativo o la oficina para satisfacer sus necesidades diarias de agua. Con su diseño refinado y tamaño pequeño, es la mejor opción para un apartamento de alquiler.

grifos de ósmosis

TOPWAY Ósmosis Inversa del Grifo del Fregadero de la Cocina del Grifo del Agua Potable de 360 Grados Gire la Sola Palanca Acero Inoxidable, para Todos Sistemas Ósmosis Inversa Filtración del Agua
- Hecho de acero inoxidable chapado en cromo
- Perfecto para fregaderos de doble tazón
- Mango grueso y suave
- Cómodo de usar y cómodo de usar


Ibergrif, M22301A, Grifo de Osmosis Inversa, Grifo de Cocina Agua Potable, Acero Inoxidable, Giratorio 360 grados, Grifo de Osmosis Inversa con Adaptador de 2, Grifos, Plata
- Material de alta calidad
- Mango único de 90 grados salida de agua giratoria de 360 grados
- Diseño brillante Hay una delicada superficie procesada con un color elegante y un diseño elegante, lo que puede ser una decoración perfecta para su cocina
- Uso general El grifo de agua nuevo y de alta calidad se usa ampliamente en varios tipos de agua pura, filtros de agua
- Fácil de instalar se adapta a todos los sistemas de filtro de agua debajo del mostrador, que es fácil de instalar


JTLB Wer Kitchen 32 * 15 * 4 1/4 ''aleación de Zinc Grifo de Cocina Grifo Cromado ósmosis Inversa RO Filtro de Agua Potable
- Fácil de mantener El acabado oxidado superior resistente a la corrosión evita que la suciedad se adhiera a la superficie del grifo, limpiar el grifo con un paño es suficiente en el uso diario.
- Construcción de material premium Grifo de baño monomando resistente y fiable. Hecho de aleación de zinc de primera calidad con superficie cromada, es resistente y elegante para un largo tiempo de servicio.
- Grifo de cuello de ganso con diseño de rotación 360 fácil de usar.
- Material de alta calidad Este grifo de cocina está hecho de acero inoxidable de alta calidad y es duradero.
- . Material Premium Hecho de aleación de zinc de alta calidad, resistente y duradero.


Grifos Cocina Fregadero, CECIPA Grifo Osmosis 3 Vías con 2 Salidas, Grifo de Cocina para Agua Potable con Palanca Doble, Giratorio de 360°, Acero Inoxidable Cepillado
- 💖GRIFO COCINA 3 VíAS: Este grifo cocina puede suministrar agua fría, agua caliente y agua filtrada. Al conectar un dispositivo osmótico o un sistema de filtro de agua, el agua se puede purificar para reducir el contenido de incrustaciones y metales pesados, lo que da como resultado agua potable. Solo necesita preparar 1 orificio de montaje, ahorrando espacio,CECIPA PURE grifo osmosis satisface sus necesidades!
- 💖MANIJAS DOBLES & SALIDAS DOBLES: La manija de agua derecha controla el agua fría y caliente, la manija izquierda controla la purificación del agua. Las dos asas son independientes entre sí, lo que satisface exactamente sus necesidades de agua. El grifo de cocina tiene dos salidas de agua y 2 núcleos de válvula de cerámica, el agua purificada y el agua del grifo pasan por tuberías y salidas independientes, por lo que la calidad del agua no se verá afectada entre sí.
- 💖USO FLEXIBLE: El diseño de boquilla de grifo fregadero de radio amplio y alto tipo "L", la altura de la salida de agua es de 310 mm, lo cual es conveniente para limpiar la olla y acomodar botellas grandes. El grifo osmosis cocina giratorio de 360 grados se adapta a cualquier fregadero simple o doble, conveniente para limpiar cualquier esquina.
- 💖HERMOSO & DURADERO: El cuerpo de acero inoxidable de este grifo osmosis 3 vias es más duradero y no se tambalea. La tecnología de superficie de acero inoxidable cepillado puede resistir la corrosión en el uso diario y es más resistente a los rayones y las manchas de aceite. El aspecto clásico de PURE grifo 3 vias se adapta elegantemente a cualquier estilo de cocina. Por su salud, le prometemos que todas las piezas mecanizadas cumplen con los requisitos para la certificación no tóxica.
- 💖SUMINISTRAREMOS: 1 × Grifo cocina 3 vias, 2 ×mangueras de agua fría y caliente de 60 cm (G3 / 8 "), 1×G3/8" (60 cm) Manguera de agua potable con conexión de 1/4", 1 ×aireador libre de 22 mm, 1 ×placa de montaje de plástico, juego de accesorios de instalación e instrucciones. Si tiene alguna pregunta al instalar y usar el grifo, puede contactarnos en cualquier momento y nos comunicaremos con usted dentro de las 24 horas.

sistemas de ósmosis
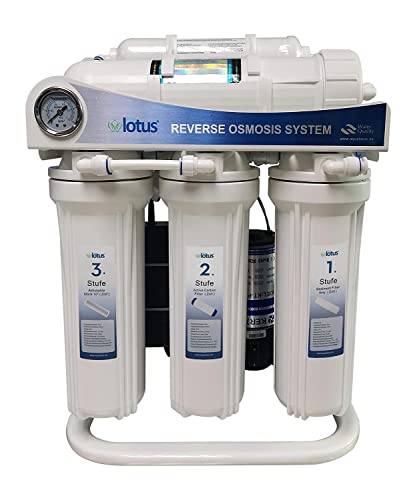
Sistema de ósmosis 600 GPD Perfect Water Direct Flow sin necesidad de tanque, filtro de agua de ósmosis inversa, filtro de agua potable, ósmosis inversa
- Potencia: aprox. 1,6 litros por minuto de agua de ósmosis más pura de una membrana de alto rendimiento de 600 GPD
- ✅ Reemplazo de cartuchos de filtro de 10 pulgadas. Intervalos de cambio recomendados para pre-y post-filtro: 3-6 meses, membrana: 12-24 meses.
- Seguro: cualquier contaminante, como bacterias, virus o nitratos y metales pesados se eliminará de forma segura. El agua no tiene cal.
- Datos técnicos: dimensiones: 50 cm x 37 cm x 22 cm (alto x ancho x profundidad), presión del agua mínima. 1, máx. 4 bar, conexión de entrada de agua de 1/2 pulgadas
- Eficaz: menos costos de aguas residuales con una relación de hasta 1:1. Planta Directflow sin depósito
- ✅ Filtro de repuesto - https://www.amazon.de/dp/B09Q1L257S?ref=myi_title_dp


ATH - Osmosis Inversa 5 Etapas Genius Pro 50 + Recambios Osmosis Originales

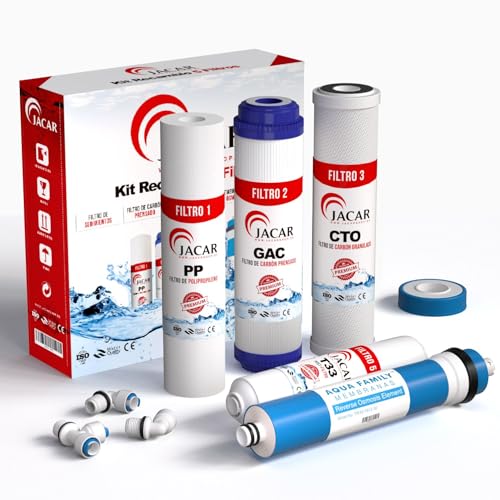
JACAR - Pack Membrana + Filtros de Ósmosis Inversa de 5 etapas Universales | Compatible con todos los sistemas de ósmosis | Recambios de filtros depuradores de agua
- 🔴 FILTROS DE OSMOSIS INVERSA PARA 1 AÑO: Nuestro paquete incluye los 4 filtros esenciales y una membrana de alta calidad de 50 GPD, junto con terminales y teflón. Con este kit de filtros de osmosis completo, disfrutarás de la tranquilidad de tener agua de calidad en tu hogar durante 12 meses sin preocuparte por recambios constantes.
- 🟢 COMPATIBILIDAD 100% CON TODAS LAS MARCAS DE OSMOSIS INVERSA: Nuestros filtros son perfectamente compatibles con el 100% de los sistemas de osmosis inversa NO COMPACTAS (consulta la foto número 3 para identificar los equipos no compactos).
- 🔵 BENEFICIOS: Ideal para cocinar y lavar tus alimentos para evitar los componentes nocivos que entren en nuestro organismo. Evita la cal en tus electrodomésticos como cafeteras, planchas, vaporeras, acuarios, etc. Para los deportistas, se acabó comprar agua embotellada.
- 🟡 ENCUENTRA INSTRUCCIONES DETALLADAS Y ESQUEMA DE MONTAJE: Puedes consultar nuestras instrucciones y el esquema de montaje detallado. Más abajo encontrarás más fotos en las cuales te explicamos lo fácil y sencillo que es el proceso de instalación para que lo puedas hacer tú mismo.
- 👀 GARANTÍA DE SATISFACCIÓN 100%: Estamos tan seguros de la calidad de nuestros filtros de osmosis que ofrecemos una GARANTÍA DE SATISFACCIÓN COMPLETA. Si no estás completamente satisfecho con tu compra, te garantizamos un reembolso total o un reemplazo.


Geekpure Sistema de filtro de agua para osmosis inversa de 6 etapas con pH mineral alcalino + filtro de reiniciación 75GPD
- Tecnología avanzada: filtra hasta 0.0001 micrones. Elimina arsénico, plomo, fluoruro, mercurio, cadmio, olores, metales pesados y más de 1000 contaminantes
- El sistema de Ro regular produce un pH de agua ligeramente ácido a 5-6.5. Esta unidad incluye un filtro de remineralización alcalina de sexta etapa adicional que ajusta el pH del agua pura a 7.5-8.5
- Los componentes de primera calidad garantizan la máxima fiabilidad y un bajo mantenimiento durante muchos años. Todos los tubos, accesorios de empuje rápido, tanque de almacenamiento, membrana Ro tienen certificación NSF, para proporcionar agua pura y saludable. Grifo del fregadero de cocina de lujo SIN PLOMO como última garantía de agua pura en su hogar
- Capacidad del sistema 75 galones por día a 60 psi. Capacidad del tanque 2.8 galones, se adapta a la mayoría de los gabinetes debajo del fregadero, tamaño inteligente para garantizar que obtenga agua pura en todo momento. Tamaño de la tubería: 1/4 pulgadas y 3/8 pulgadas. La proporción de agua pura y aguas residuales es 1: 2. Condición del agua de alimentación: Presión del agua: 40-100 psi, Templado: 40-110 ° F / 5-45 ° C, Ph: 3.0 -11.0, TDS máximo: 2000 ppm de agua del grifo o agua de pozo
- El sistema viene con accesorios de conexión rápida, tubos codificados por colores y videos para una fácil experiencia de bricolaje.No pierda dinero en una instalación profesional, puede comprender todo sobre su sistema e instalarlo con nuestras instrucciones bien organizadas en un par de horas.
